实现小鼠体内高效编辑!
李大力团队开发基于IscB的高活性迷你基因编辑工具
在过去十多年里,以CRISPR/Cas9为代表的基因编辑及其衍生技术得到了快速发展,使人们能够更加精准高效的对基因进行改造,为更好的理解生命过程、开发精准的基因疗法提供了新的可能性。首个基于CRISPR/Cas9技术的离体(ex vivo)基因编辑疗法Casgevy已于2023年底获批上市,用于地贫和镰贫的基因治疗【1】;通过肝脏靶向的LNP-mRNA递送的方式,在体(in vivo)基因疗法也取得了喜人的临床试验数据。基因编辑技术已经迈进了临床应用的时代。然而,靶向于肝脏以外器官的在体基因编辑治疗仍存在很大的瓶颈。目前适用于肝外基因递送的载体主要是腺相关病毒(Adeno-associated viruses, AAV),然而其包装上限约4.7kb,单个载体难以递送Cas9等核酸酶及其衍生编辑系统。因此寻找小尺寸、高效率的基因编辑系统对于实现安全高效的体内递送具有重要意义。近年来,陆续报道了一系列小型Cas蛋白,包括小型Cas12f蛋白【2-4】、其进化上的祖先TnpB【5, 6】以及真核同源物Fanzor【7, 8】。
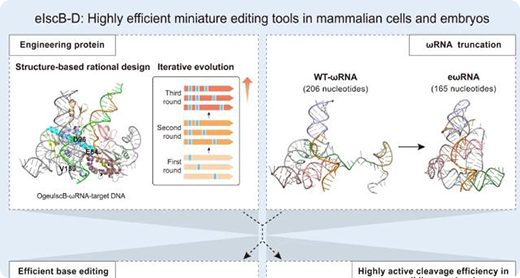
然而,由于Cas12f家族只有一个RuvC结构域,难以用于碱基编辑、先导编辑等依赖于缺口酶的衍生技术。 2021年,张锋团队通过对测序数据有针对性的挖掘和分析,发现由IS200/IS605转座子超家族编码的IscB核酸酶,也具有能够切割DNA链的HNH和RuvC结构域【9】。作为Cas9可能的进化祖先,IscB普遍只有约400-500个氨基酸(仅为SpCas9氨基酸长度的三分之一左右)利用一段非编码RNA(ωRNA)引导蛋白识别切割DNA。因此,IscB更有潜力构建缺口酶,与胞嘧啶脱氨酶(APOBEC)、腺苷脱氨酶(TadA)或逆转录酶(RT)融合,构建可由单个AAV完整包装的迷你碱基编辑器(BE)或先导编辑器(PE),具有极大的临床应用潜力。然而,IscB在哺乳动物细胞中的活性非常有限。以OgeuIscB为例,其在HEK293FT细胞中编辑效率不到5%。因此,能否通过工程化的改造提高IscB的基因编辑活性,达到与Cas9相当的活性是需要解决的首要问题。 2024年8月2日,华东师范大学李大力团队在Molecular Cell上发表题为:Engineering IscB to develop highly efficient miniature editing tools in mammalian cells and embryos 的研究论文。该研究综合蛋白质工程化改造、RNA结构优化、胚胎注射等技术,成功获得在人类细胞以及鼠源细胞系中具有超高编辑活性的IscB变体(eIscB-D)。通过将IscB切口酶(eIscBH339A)与腺苷脱氨酶(TadA-8e)或胞嘧啶脱氨酶(hA3A*)融合,开发出超高活性的迷你单碱基编辑器eiABE和eiCBE。该系统在小鼠胚胎中展现高效的体内编辑活性,可用于构建白化病等疾病动物模型。 为了提高IscB蛋白活性,研究者基于结构理性设计在关键位置引入精氨酸突变【10, 11】,经过三轮迭代筛选,成功获得增强型IscB(命名为eIscB)。eIscB相较于野生型IscB编辑效率最高可以提升22.4倍,平均编辑效率可提高7.5倍。此外,研究者通过融合一个非序列特异性DNA双链结合蛋白(HMG-D)提高了IscB与目标DNA的亲和力,高活性IscB(eIscB-D)的最高编辑效率可达91.3%。在此基础上,研究者针对向导RNA进行优化改造,获得高效ωRNA(命名为eωRNA),且长度相较于野生型ωRNA缩短了约20%,降低了工业合成的难度。最后优化获得的eIscB-D/eωRNA编辑效率相比原始IscB/ωRNA平均可提升20.2倍。
接下来研究者通过在RuvC结构域关键催化位点引入丙氨酸突变,通过筛选,开发了IscB切口酶(eIscBH339A),并与腺苷脱氨酶(TadA-8e)和胞嘧啶脱氨酶(hA3A*)分别融合开发出超高活性的迷你单碱基编辑器eiABE和eiCBE,最高位编辑效率分别可达到73.6%和79.2%。 此外,先前并没有研究证明IscB在小鼠体内可以产生高效编辑。研究者首先在小鼠N2a细胞系中针对PCSK9以及Tyr基因进行靶点筛选。测序结果表明eIscB-D在PCSK9-sg29这一靶点可实现58%的编辑效率,在Tyr-sg21靶点的编辑效率为47.1%。研究者随后通过胚胎注射eIscB-D/eωRNA系统靶向Tyr基因的1号外显子,破坏白化基因的表达,成功制备小鼠白化疾病模型。在F0代,75%(9/12只)突变小鼠实现高效编辑(平均编辑效率为58.8%),其中有5只产生编辑效率接近100%的完全白化表型。该研究首次证明了eIscB-D不仅可以在鼠源细胞系中产生高效编辑,并且可以通过胚胎注射高效制备疾病动物模型。 总的来说,该研究成功开发了基于IscB的高活性迷你基因编辑工具,率先实现了小鼠体内高效编辑。该研究极大增加了单个AAV载体安全高效递送碱基编辑或者先导编辑系统的可能性,丰富了基因编辑工具的应用场景,为将来用于体内基因治疗提供了高效的候选技术。 华东师范大学博士研究生薛念念,硕士研究生洪迪珊,博士后张丹以及硕士研究生王茜为本文的共同第一作者,华东师范大学为第一单位,华东师范大学李大力研究员,朱一凡、王立人副研究员为本文的共同通讯作者。华东师范大学生命科学学院刘明耀教授,宋高洁研究员、关玉婷研究员、新加坡国立大学胡纯一教授等对本项研究提供了重要支持。


